
电话:
021-67610176传真:
在弗吉尼亚联邦大学梅西癌症中心,科学家正在进行一项可能改变细胞免疫治疗方式的基础研究,该项目获得弗吉尼亚联邦大学梅西癌症中心(VCU Massey)试点资助。该项研究从的定量角度分析了免疫系统如何响应细胞疗法,从而寻求一种新的细胞免疫治疗方式,干细胞移植和CAR-T细胞疗法的协同作用。该研究建立了数据模型模拟了细胞免疫疗法中的免疫反应。

“我们已经建立了干细胞移植和依赖免疫系统的其他形式的癌症治疗中观察到的免疫反应的模型,”Massey血液学家、肿瘤学家和研究员AmirToor医学博士说道:“这让我们了解免疫移植和肿瘤免疫治疗后发生的反应是一种确定性而非随机的过程。未来,我们希望这些模型用于治疗决策,这将改善血液和淋巴系统癌症患者的治疗结果。 “
模型的建立
Toor博士一直致力于建立免疫反应的建模。
人白细胞抗原(HLA)是指编码负责调节免疫系统的细胞表面蛋白质的基因。目前,医生使用HLA检测来匹配干细胞供体和具有相似HLA组成的受体。HLA基因产生的蛋白质有助于身体的免疫系统区分哪些细胞是“自我”的,哪些细胞是外来的。
研究人员研究了干细胞移植供体-受体的次要组织相容性抗原(mHA)的变异。mHA是HLA分子上呈递的蛋白质片段,其与免疫系统T细胞上的受体相互作用。研究人员使用先进的基于计算机的分析,研究了mHA与HLA之间的潜在相互作用,并发现干细胞移植供体-受体中mHA的高水平变异。这种变异可能导致移植物抗宿主病(GVHD),这是一种可能危及生命的并发症,其中供体的免疫细胞在移植后攻击受体中的健康组织。
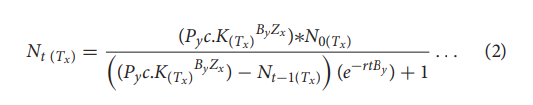
模型公式
该模型原理是根据mHA相互作用和供体与受体之间的蛋白质编码差异。科学家证实, T细胞反应的程度与患者累积的GVHD发生率相关。
“我们相信该种类型的模型可用于确定移植受者的供体,降低移植物抗宿主病等并发症的风险。并且,它也可能为移植后的免疫抑制剂量提供信息,”Toor表示。
模型在CAR-T上的应用
在近发表在“ 骨髓移植 ”杂志上的第二项研究中,Toor将项研究用于CAR-T细胞疗法。在这项研究中,研究人员得出了一个数学公式,可用于开发变化的剂量参数。计算CAR-T细胞治疗的剂量,可以监测细胞因子释放综合征的严重性,细胞因子释放综合征是由CAR -T细胞和肿瘤细胞的相互作用引起的潜在致命的免疫应答。
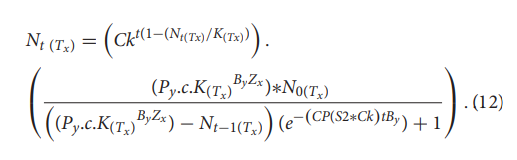
模型公式
“我们证明,有可能在数学上推导出CAR-T细胞扩增与目标白血病细胞生长之间的关系,”Toor说。“这将有助于医生建立特定患者肿瘤负荷的剂量参数,以限制药剂毒性。”
近发表在“ 免疫学前沿 ”杂志上的后一项研究进一步应用了之前的模型。Toor和他的团队考虑了干细胞移植中存在的其他变量,这可能有助于更准确地模拟供体和受体之间的T细胞反应。
结语
“通过这项研究,我们开发了一个全面的免疫反应数学框架,为各种对T细胞免疫学至关重要的因素提供了新的视角。这些模型坚定地证明免疫反应不是随机的,而是可以计算和预测的,”Toor说。“我们将医疗应用于干细胞移植和肿瘤免疫疗法在概念上得到突破。”
研究人员正在继续改进他们的模型,同时努力确保资金使他们能够通过使用全外显子组测序来评估和治疗在梅西癌症中心接受细胞治疗的患者。他们未来的工作将研究这些DNA序列谱库差异如何在移植后改变供体免疫细胞谱,将其塑造成受体的组织抗原谱。该研究结果将为医生提供实时测量免疫反应和对治疗进行适当调整。(生物谷)
参考来源:
Ali Salman,Vishal Koparde,Charles E. Hall,Max Jameson-Lee,Catherine Roberts,Myrna Serrano,BadarAbdulRazzaq,Jeremy Meier,Caleb Kennedy,Masoud H.Manjili,Stephen R.Spellman,DayanjanWijesinghe,Shahrukh Hashmi,Greg Buck, Rehan Qayyum,Michael Neale,Jason Reed,Amir A. Toor。 Determiningthe Quantitative Principles of T Cell Response to Antigenic Disparity in StemCell Transplantation. Frontiersin Immunology, 2018; 9 DOI: 10.3389/fimmu.2018.02284
文章中图片公式均来自上述文献